İlk olarak, yorumlarda belirtildiği gibi diyagramlar açısından her iki diyagram da doğrudur. Her iki diyagramın da ima ettiği bir şey, süblimasyon / biriktirmenin erime / donma ve buharlaşma / yoğunlaşma kombinasyonuna eşdeğer olmasıdır - buna bakmanın başka bir yolu da UC Davis ChemWiki sayfasındaki Süblimasyon Isısı:
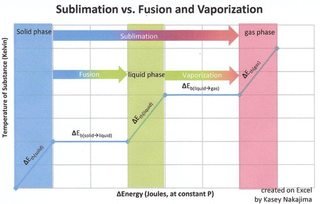
Web sayfasından bir açıklama şudur:
Süblimasyonda sağlam bir Gaz fazına giderken sıvı fazdan geçmez, önce eriyeceği (kaynaşacağı) ve sonra buharlaşacağı miktarda enerji alır.
Sizinle ilgili olarak sorular:
Bunun nedeni bazı maddelerin sıvı olamaması mıdır? eğer öyleyse sıvı olmasını engelleyen nedir?
Tam olarak değil, doğru koşullarda sıvılar oluşabilir, açıklama aşağıdadır.
Neden süblimasyon sırasında ve biriktirme sıvı fazın atlanmasıdır ve nasıl atlanır, tüm maddelerin katı ve gaz arasında sıvı olması gerekmez mi?
Süblimasyonun neden gerçekleştiğini anlamak için faz diyagramlarının anlaşılması gerekir . UC Davis Chemwiki sayfasından Faz Diyagramları 'ndan genelleştirilmiş bir faz diyagramı aşağıda gösterilmektedir:
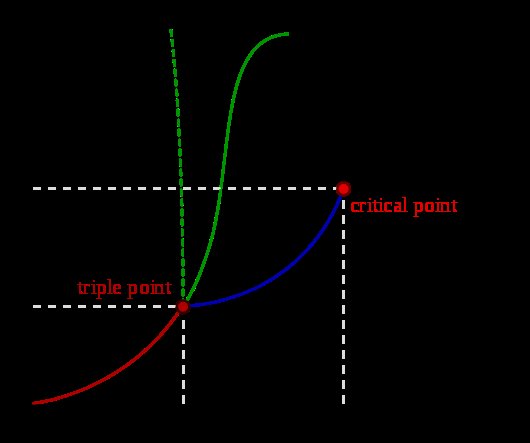
Süblimasyon / biriktirme eğrisi, başlangıç noktasından gelen çizgidir yukarıdaki diyagramda kırmızı çizgi olarak gösterilen üçlü noktaya. Yapılabilecek bir genelleme, bir maddenin, sıcaklık ve basınçtan biri (veya her ikisi) üçlü noktadan daha düşük olduğunda süblimleşme / birikmeye maruz kalmasıdır. Karbondioksit ve suyun faz diyagramlarını karşılaştıran aşağıdaki örnekleri göz önünde bulundurun (daha önce bağlantısı verilen UC Davis Chemwiki sayfasından):
İlk olarak, karbondioksit - 'normal' atmosferik basınçta (tipik laboratuvarda olduğu gibi - 1 atm), üçlü noktada ('D' olarak etiketlenir) 5,2 atm'den daha düşüktür. Standart laboratuvar koşullarından minimum basınç değişiklikleri olduğu varsayılırsa, $ \ ce {CO2} $ soğudukça, sonunda katı faza geçecektir.
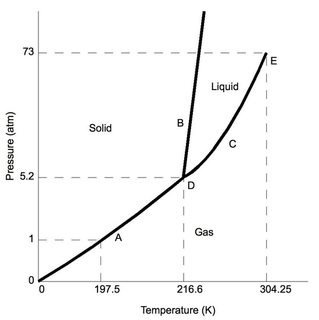
Şimdi, Karşılaştırma için, su için faz diyagramını göz önünde bulundurun, üçlü durum ('D' olarak da adlandırılır) 0.006 atm çok düşük bir basınçta meydana gelir, bundan daha düşük basınçlar su süblimleşmesine neden olur. Standart laboratuvar koşulları için su, bilinen katı, sıvı ve gaz özelliklerini korur (sıcaklığa bağlı olarak).
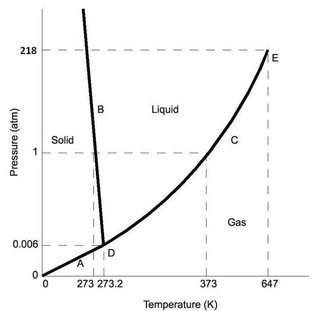
Not, her ikisinin de sıvı fazı vardır.